近年来,随着“临床治愈”概念的普及,乙肝的临床治疗愿景正在发生变化,而更重要的是,对于乙肝新药研发企业而言,“完全治愈”或许已不再是终极追求。
2015年我国《慢性乙型肝炎防治指南》首次提出“临床治愈”概念,而2022版的《慢性乙型肝炎防治指南》也进一步明确,对于部分适合条件的慢性乙肝患者,应追求临床治愈。
2023年11月17日,国家卫生健康委医院管理研究所面向全国启动“乙肝临床治愈门诊规范化建设与能力提升项目”,计划到2025年,在全国建设超过百家乙肝临床治愈门诊,实现乙肝诊疗、临床治愈网络广覆盖。
2024年7月,国家卫生健康委医院管理研究所公布23个省份的35家医院作为第一批规范单位,并确定147家医院为第一批项目培育单位,表现出乙肝“临床治愈”门诊的重大建设意义。
很明显,无论是理念宣传,还是相关基础建设,“临床治愈”都正在成为现阶段乙肝治疗的终极追求。
但为何,明明乙肝“临床治愈”无法从根本上消除乙肝患者肝癌化的风险,却仍能有如此地位,对于患者与新药研发企业而言,“临床治愈”又到底意味着什么?
从“部分治愈”到“临床治愈”
其实,原则上,乙肝应该是病毒领域机制最复杂的疾病,之所以发现近60年仍无法被攻克,其主要是病毒双链DNA能在细胞核中形成cccDNA,除常规中心原则下转录为RNA、形成病毒蛋白的同时,还能通过前体RNA逆转录形成双链DNA,最后双链DNA与病毒蛋白再次组成新的病毒颗粒,开始新一轮的感染。
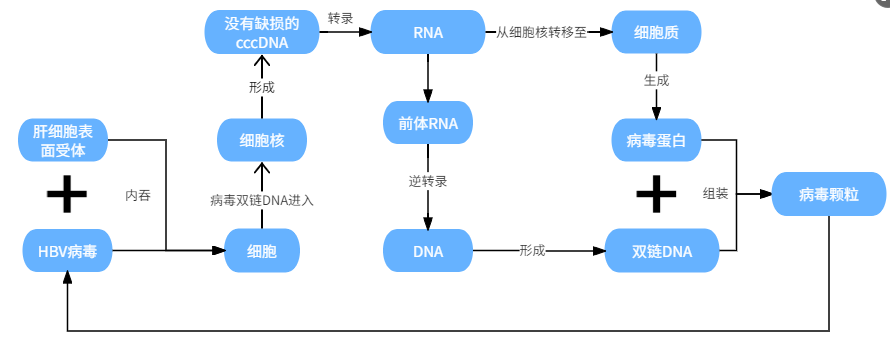
巨量的病毒颗粒,最终让免疫细胞疲于应付,压制免疫系统,使得人体难以形成有效的抗体。而对于乙肝病毒治疗,早年间虽无法从致病机制上达到治愈的目的,但通过控制乙肝病毒的复制,临床上也基本能达到乙肝的“部分治愈”。
以恩替卡韦、替诺福韦为代表的病毒抑制疗法是该阶段“病毒欺骗”理念的重要代表,作为一种核苷酸类似物,其可以在乙肝病毒逆转录酶蛋白的过程中,替代核苷酸,导致乙肝DNA发生错误,继而中断其复制过程。
但是,由于核苷类药物只能作用于逆转录阶段,虽能促进部分乙肝患者出现HBsAg的丢失,却存在着四大核心弊端:
1.患者需要长期服药,断药复阳概率大。
2.无法清除肝内cccDNA与HBVDNA,肝癌的发生风险并未完全消除。
3.临床治愈效果有限,单用NAs治疗实现HBsAg清除率仅为0~3%/年。
4.治疗存在优势人群,即HBsAg水平>1500IU/ml患者不适用。
后续,随着干扰素在乙肝治疗作用被发掘,临床上主流的治疗方案也逐渐从单药治疗,转向了联合治疗,最显著的代表即核苷类药物+干扰素。但其总体治愈率也仅有30%-50%,且随着HBsAg水平上升,其临床治愈率也呈反向下降趋势。
因此,对于乙肝的临床治愈,在原有“NAs+干扰素”联合治疗的基础上,临床上迫切需要一种能弥补上述局限性的全新疗法,即
1.可以适用于HBsAg高水平患者(大于1500IU/ml);
2.临床治愈率远高于现有30%—50%水平;
3.作用机制上能清除cccDNA,将肝癌风险降至0;
4.不需要长期服药,患者顺应性较高;
小核酸领域的ASO与RNAi就是现阶段最受期待的创新疗法之一,也被誉为乙肝最有希望实现“功能性治愈”的疗法。
创新疗法丛生,
“RNA疗法”引领未来
在专业领域上来讲,乙肝的真正治愈可以分为两种,即临床治愈与完全治愈。
临床治愈,是指治疗后的HBsAg检测阴性,血中HBV-DNA消失,即以临床症状消失、肝功能正常为主要目的。
完全治愈,则是指HBsAg检测阴性的同时,血与肝脏中的HBV-DNA消失,能清除肝脏中的共价闭合环状DNA(cccDNA),使乙肝患者肝癌风险降低至0。
以目前的研究水平,乙肝的“完全治愈”还无法实现,但针对不同的临床期许(HBsAg高水平适用、高临床治愈率,能清除cccDNA等),临床上已有超过200余款乙肝新药正在抓紧推进,现阶段乙肝适应症新药主要分为直接抗病毒药物、间接抗病毒药物与其他三类。

其中,直接抗病毒药物作为乙肝治疗的主力,目前主要研究方向集中在病毒进入抑制剂、衣壳抑制剂、HBsAg抑制剂、反义寡核苷酸(ASO)、RNA干扰剂与基因治疗等方向,衣壳抑制剂与RNA干扰疗法占比最大,是海内外药企研发的主要突破方向。
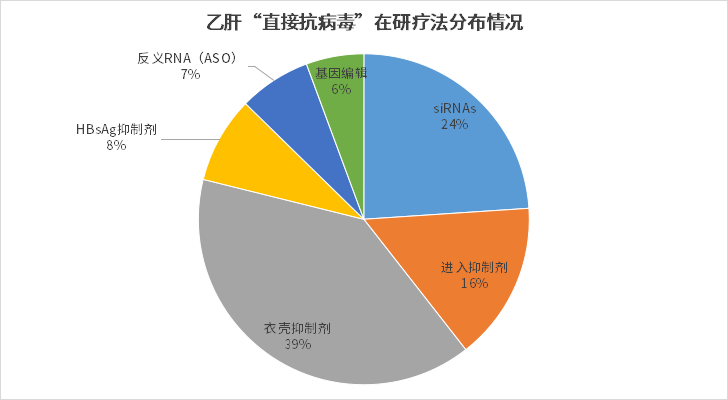
衣壳抑制剂:
其机制上是通过诱导核心蛋白的异构变化来抑制HBV衣壳,从而导致非感染性病毒颗粒(空核衣壳)形成,继而无法完成后续的逆转录和复制环节,临床作用上与当初早年间的核苷类似物类似,但其在降低病毒DNA的同时,还能降低RNA。
从目前新药研发格局上看,衣壳抑制剂是毫无疑问的乙肝新药集中地,且绝大多数研究进度靠前的管线均来自国内,比如东阳光的甲磺酸莫非赛定、齐鲁制药的QL-007、药明康德与广生堂的GST-HG141等。

但是,衣壳抑制剂由于本身作用机制的原因,导致其虽具有一定临床优势,却也存在较大的弊端,即无法实现表面抗原转阴。以甲磺酸莫非赛定(GLS4)为例,其Ⅱ期结果中,虽然其联合恩替卡韦在降低HBVDNA、pgRNA、HBsAg和HBeAg的幅度显著优于恩替卡韦单药,但其HBsAg下降方面相比恩替卡韦单药却并无优势。
而恰好,判断一款药物在治愈HBV上是否有潜力,能否有效降低HBsAg正是关键,这也就导致绝大部分衣壳抑制剂新药现如今尴尬的研发局面。
不过,另一款来自Aligos的新型衣壳抑制剂ALG-000184,其最新研究结果显示,其不仅能实现HBVDNA和RNA水平的有效下降,在HBsAg的水平降低上也显示出一定的疗效,甚至还可能存在降低cccDNA水平,或许是去除整合HBVDNA的作用。
这也侧面证明,核衣壳抑制剂对病毒的抑制可能是多种机制共同作用的结果,随着更多作用机制的探索与发现,领域内新药或还需迭代升级。
RNA干扰疗法:
相较衣壳抑制剂而言,RNAi药物在作用机制上则存在较为明显的优势,其高效靶向和降解HBV转录的本质,可以抑制HBV抗原表达,阻断病毒复制,减轻免疫耐受,虽然对cccDNA或整合病毒DNA无直接作用,但却可以抑制来自整合HBV-DNA和cccDNA的HBsAg。是目前有望在临床实践中实现“功能性治愈”的疗法。

并且,RNA干扰疗法也是现阶段乙肝直接抗病毒疗法中研究数量仅次于衣壳抑制剂的存在,粗略统计,全球约有17款重点管线涉及,其中腾盛博药的VIR-2218、GSK的JNJ3989既是领域内研究进展最快的企业,也是国内唯二获得突破性疗法的产品。
2023年欧肝会上,VIR-2218公布的II期临床数据显示,VIR-2218联合干扰素48周时,表面抗原转阴且表面抗体阳性的比例为30%,停止24周的HBsAg清除率仍有15%左右,也就是功能性治愈比例为15%。并且治疗结束时anti-HBs水平〉500mIU/mL的受试者100%维持HBsAg清除。
虽然上述数据已是目前RNAi治疗乙肝的最优数据,但较少能实现HBsAg清除仍困扰着领域发展,目前联合疗法之后的鸡尾酒疗法或将成为突破的关键,也是目前乙肝新药领域最有希望实现真正意义上的“功能性治愈”的领域。
结语
其实,对于乙肝的创新疗法而言,除了衣壳抑制剂与RNA干扰疗法外,领域内还有不少创新疗法在研,就现阶段而言,谁也没法确定乙肝的终结者会是谁。
但可以确定的是,未来5-10年内,随着RNAi、ASO等治愈性疗法接连上市,加之婴儿乙肝疫苗的普及率上升,乙肝患者的数量与严重程度一定会呈反向下降。
这对于相关医药企业来讲,或许并非一件好事,而更关键的是,那些以乙肝“完全治愈”为目标的企业还能剩下多少意义?
或许,期望中的“完全治愈”疗法,永远不会到来。





临床治愈门诊只不过是在割韭菜罢了,三成不到的概率,一个疗程几万块[笑着哭]
资本比乙肝更可怕,,