作者:李春燕 常杏 黄爱萍 汤善宏
单位:西部战区总医院消化内科
编者按:为了帮助临床肝病医生扩宽视野、丰富实践,培养临床思维能力,《国际肝病》特邀请西部战区总医院消化内科汤善宏教授团队共同打造“Liver疑难病例”专栏。本栏目汇集了汤善宏教授团队多年临床诊治工作中所遇到的“经典病例”,同时也将定期搜集知名学术期刊所刊发的或复杂或罕见的临床病例,重点阐述各种肝病的诊疗思路,为广大同道提供宝贵的临床借鉴。
主题述评肝脾肿大、胆汁淤积及脾梗死病因多变,临床诊疗具有一定困难。而同时合并以上三种症状的诊疗更具挑战。弥漫性大B细胞淋巴瘤(diffuse large B cell lymphoma,DLBCL)是非霍奇金淋巴瘤中最常见的组织学类型,其病变侵犯全身各系统脏器,缺乏特异性。以肝脾肿大、脾梗死、胆汁淤积为主要表现的DLBCL在临床上较为罕见。本文主要报道1例以肝脾肿大、脾梗死、胆汁淤积为主要表现,后病情急剧恶化发展为淋巴瘤相关噬血细胞综合征、肝功能衰竭、肠道功能衰竭的DLBCL病例,从而为临床工作者对于该类疾病的诊治提供一些新的思路。
病历摘要患者男性,主因“反复颈部疼痛3月余,腹痛、腹胀8天”入院。3月余前患者出现颈部淋巴结肿大、疼痛,于院外就诊,予以对症治疗(具体不详)后患者颈部肿痛减轻,自诉肿大淋巴结消失。住院期间(8天前)无明显诱因出现腹痛、腹胀,呈持续性隐痛,放射至后腰背部,伴头晕、乏力,伴皮肤巩膜黄染、恶心、呕吐、纳差,辗转于两家医院就诊。
2024-04-15院外查肝功能:ALB 35.2 g/L、ALT 36 IU/L、AST 148 IU/L、TBIL 121.12 μmol/L、DBIL 90 μmol/L、IBIL 31.12 μmol/L、γ-GGT 489 IU/L、ALP 591 IU/L、TBA 94 μmol/L。腹部CT提示:1)肝脾明显增大,脾脏实质密度团片状稍低密度影;2)肝前间隙区结节影;3)腹腔内及腹膜后淋巴结增多,部分增大。给予对症治疗(具体不详)后患者腹痛较前加重,于2024-04-16入我院。
入院后查体:T 36.5℃,P 50次/分,R 21次/分,BP 129/73 mmHg,神志清楚,皮肤、巩膜重度黄染;双侧腋窝可触及肿大淋巴结,无压痛、质稍硬、可滑动;腹部稍膨隆,腹肌软,上腹部压痛明显,无反跳痛、肌紧张,全腹未触及包块,肝脏下缘至肋缘下6横指,脾下缘至肋缘下4横指,胆囊未触及明显异常,墨菲征(-),移动性浊音(-),肝区叩击痛(-),双侧肾区叩击痛(-)。肠鸣音2次/分,未闻及振水音及血管杂音。
辅助检查:血常规+CRP:WBC 8.92×1012/L、RBC4.46 ×109/L 、HCT 40.7%、PLT 27×109/L↓、N 4.50×109/L、N% 50.5%、L 3.32×1012/L↑、CRP 27.10 ng/L↑;凝血功能+D-二聚体:PT 13.1 S↑、APTT 38.9 S↑、TT 36.5 S ↑、INR 1.14、D-二聚体 5.85 ng/L↑;肝功能:TBIL 143.1 μmol/L↑、DBIL 90.9 μmol/L↑、IBIL 52.4 μmol/L、ALT 36.1 IU/L、AST 197.6 IU/L↑、GGT 824.3 IU/L↑ 、ALP 591 IU/L↑、TBA94 μmol/L↑;肝炎病毒: HBsAg(+)、HBsAb(+)、HBeAb(+)、HBcAb(+),其余阴性;HCV Ab(±);HBV DNA < 2.0×102 IU/mL;HCV RNA<5.0×102 IU/mL;肿瘤标志物:CA125 493.20 U/mL↑、CA199 242.90 U/mL↑;尿常规:胆红素3+、尿胆原4+、尿蛋白+-。
完善腹部增强CT提示(图1):(1)十二指肠降段-水平段交接区团块软组织密度影,增强后强化后与肠道一致,考虑肠道聚集所致;(2)肝脾肿大,脾脏内斑片及楔形低密度影,强化不明确,考虑脾梗死可能;(3)肝前间隙、左心膈角区、肝胃间隙、腹腔及腹膜后多发肿大淋巴结显示;(4)直肠-乙状结肠交界区上方肠管积气、积液扩张并部分气液平形成。

图1. 腹部增强CT示:脾脏体积明显增多,实质内多发斑片及楔形低密度影,增强后强化不明显(A矢状位动脉期,C为冠状位动脉期),脾门处见径约2.5 cm结节状软组织低密度影(B图矢状位门脉期,D为冠状位门脉期)
予以抗感染、通便、保肝、退黄、维持电解质平衡及营养支持等治疗,效果欠佳,患者腹痛、腹胀未见缓解。进一步完善浅表淋巴结彩超示:双侧颈部II-IV多发肿大淋巴结,双侧腋窝淋巴结肿大。
后完善骨髓穿刺涂片示:有核细胞形态不清,胞核及胞膜结构模糊,呈溶解状态,无法确定细胞属性。骨髓活检病理示(图2):<骨髓>红骨髓大部分出血、坏死,背景B细胞淋巴瘤细胞侵犯。瘤细胞:Bcl-2(灶+)、CD20(+)、CD3(-)、CD5(-)、CD79a(灶+)、CD99(-)、Cyclin D1(-)、PAX-5(灶+)、TdT(-)。淋巴结活检病理示:结合免疫标记检查支持弥漫大B细胞淋巴瘤,生发中心细胞亚型(GCB)。瘤细胞:Bcl-2(+,60%)、Bcl-6(+,60%)、CD10(-)、CD20(+)、Ki-67(+,60%)、Lambda(-)、MUM-1(-)、PAX-5(+)、TdT(-)。原位杂交:EBER(-)。诊断:弥漫性大B细胞淋巴瘤。
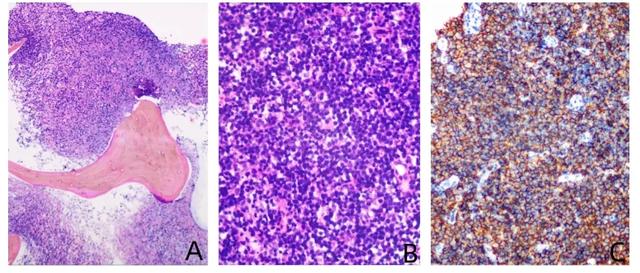
图2.(A)骨髓穿刺活检,放大倍数10×10倍,骨髓组织有核细胞容量约90%-100%,三系增生抑制伴出血、坏死,背景大量淋巴细胞弥漫浸润。(B)腋窝淋巴结活检,放大倍数1×20倍,镜下为中等大小的淋巴细胞弥漫均匀分布。(C)淋巴结穿刺活检免疫组合CD20,放大倍数10×20倍
住院的第5天开始出现连续发热,最高体温39.5℃,住院的第9天发生肝性脑病,第11天出现消化道出血。2024-04-27复查血常规:WBC 0.49×109/L↓↓、PLT 5×109/L↓↓、L 0.39×109/L↓↓、N 0.04×109/L↓↓、HB 99 g/L、RBC3.20×1012/L;CRP 97.72 mg/L;肝功:ALB 25.7 g/L↓、pre-Alb 26 mg/L、TBIL 327.6 μmol/L↑、DBIL230.9 μmol/L↑、IBIL96.7 μmol/L、ALT 84.8 IU/L、AST 513.1 IU/L↑、GGT 754.2 IU/L↑ 、ALP 1044.4 IU/L↑、TBA242.9 μmol/L↑;凝血功能:TT 26.2 S↑、APTT 45.0 S↑、INR 1.47↑、PT 16.7 S↑;PCT 13.187 ng/mL↑↑。病情急剧加重,出现噬血细胞综合征、急性肝衰竭、肠道功能衰竭、重症感染、酸碱平衡紊乱等,建议重症ICU进一步多器官支持治疗,患者家属拒绝,自动出院,出院后死亡。
病例讨论脾梗死是由于脾动脉或其分支或静脉阻塞而导致的缺血坏死,其临床表现多样且具有非特异性,最常见的症状是左上腹疼痛,其他常见症状包括发热寒战、恶性呕吐和左肩放射痛。常与消化道疾病及心血管疾病相混淆,易误诊为肠梗阻、急性心肌梗死等[1]。脾梗死最常见的原因是血液系统良恶性疾病和血栓栓塞性疾病。目前引起脾梗死的血液系统疾病包括地中海贫血、白血病、淋巴瘤、骨髓纤维化、骨髓增殖性疾病、原发性血小板增多症等,最常见的是地中海贫血和恶性肿瘤如白血病、淋巴瘤。血栓栓塞疾病常见于房颤、心内膜炎、卵圆孔未闭、人工心脏瓣膜等。胰腺疾病、感染性疾病、医源性及外伤是其少见病因。胆汁淤积是肝细胞或胆管细胞胆汁生成功能障碍、胆汁分泌受抑或排泄受阻所致,常以疲劳、瘙痒、黄疸和肝功能异常为主要表现。胆汁淤积根据病变部位可分为肝内胆汁淤积和肝外胆汁淤积,病因复杂多样。
该患者为中年男性,起病急,病情进展迅速,以腹痛、腹胀为主要临床表现,查体:皮肤巩膜黄染、体表淋巴结肿大,肝脾肿大。实验室检查提示ALP、GGT、TBA、TBIL增高,影像学提示:脾脏内斑片及楔形低密度影,强化不明确,考虑脾梗死;腹腔及腹膜后多发肿大淋巴结显示。完善浅表淋巴结穿刺活检+骨髓穿刺术及流式检查后支持DLBCL的诊断,生发中心细胞亚型(GCB)。患者出现腹胀,肠鸣音减弱,腹部增强CT提示:肠道聚集、直肠-乙状结肠交界区上方肠管积气、积液扩张并部分气液平形成,考虑肠梗阻,不排除淋巴瘤浸润肠道淋巴结可能。肠梗阻导致肠道菌群及相关细菌产物易位,通过病原体相关分子模式(PAMPs)进一步损伤肝脏功能。病程中患者血三系急剧下降,炎症指标进行性升高,肝功能衰竭,予以积极抗感染、保肝、退黄等对症治疗效果欠佳,后患者出现肝性脑病、消化道出血,病情急剧加重,建议重症ICU进一步治疗,患者家属拒绝,自动出院,出院后死亡。
DLBCL临床表现多样,因累及的组织、器官和肿瘤负荷等而不同。发病初期多表现为无痛性淋巴结肿大,但DLBCL可以累及任何组织和器官,淋巴结外病变比例可达40%-60%[2]。本例DLBCL已侵犯肝、脾、肠道等结外器官。DLBCL众多的临床表现中,脾梗死是一种罕见结外病变。淋巴瘤时肿瘤细胞所致高凝状态、阻塞血管;肿瘤负荷,脾脏增长过大,导致局部组织灌注不足从而导致脾梗死[3]。早在1901年,William Osler描述早期脾梗死的临床特点为左上腹疼痛、查体脾区有压痛、伴脾脏轻度增大三联征(奥斯勒三联征)。然而Lawrence[4]等通过回顾分析26例脾梗死患者,发现约50%的患者有左侧腹痛,36%的患者有左侧腹部压痛,31%的患者脾脏区域可无任何症状及体征,并且这26名患者中,有21例患者因脾梗塞的诊断而被诊断出患有以前未被识别的潜在疾病。故脾梗死大部分可出现左腹部疼痛,但无腹痛不能完全排除脾梗死,对于诊断脾梗死患者需积极寻找病因。淋巴瘤患者出现胆汁淤积一方面是由于肿瘤细胞滞留肝脏使肝窦受压,肿瘤细胞可能会阻塞肝脏血管影响血液供应;其次,肿瘤细胞侵犯肝内胆管,导致大面积的胆管炎、胆管坏死;患者病情进行性加重,后该患者出现肝衰竭可能与后期免疫异常激活导致过度炎症反应,大量炎性细胞因子进一步损伤肝脏功能有关。
DLBCL是我国最多见的淋巴瘤亚型,侵袭性强且具有高度异质性。当进行IHC检测及FISH检测发现C-MYC阳性率≥40%、BCL2 阳 性 率≥50%,或/和BCL6 阳 性 率≥50%,即“双打击”淋巴瘤或“三打击”淋巴瘤,属于高级别 B 细胞淋巴瘤,预后不良[5]。该患者免疫组化发现瘤细胞:Bcl-2(+,60%)、Bcl-6(+,60%),但未检查C-MYC,结合患者疾病进展考虑高级别B细胞淋巴瘤可能性大。该患者病程中出现持续性发热,肝功能指标进行性恶化,血三系急剧减少,炎症指标升高,考虑合并噬血细胞综合征(Hemophagocytic lymphohistiocytosis,HLH)可能性极大,但由于患者家属要求出院,未能完善相关检查进一步明确。
《淋巴瘤相关噬血细胞综合征诊治中国专家共识(2022年版)》指出,当淋巴瘤患者出现临床上无法解释的持续发热、血细胞减少、伴脾肿大或肝功能异常时应当怀疑HLH可能[6]。噬血细胞综合征是一类由原发或继发性免疫异常导致的过度炎症反应综合征,这种免疫调节异常主要由淋巴细胞、单核细胞和巨噬细胞系统异常激活、增殖,分泌大量炎性细胞因子而引起的一系列炎症反应[7]。血清铁蛋白≥500 μg/L及可溶性白介素2受体(soluble CD25,sCD25)升高、三酰甘油>3 mmol/L和低纤维蛋白<1.5g/L是HLH诊断标准之一[8] 。细胞因子谱检测虽尚未纳入HLH的诊断标准,但白介素6(interleukin 6,IL-6)、IL-10、干扰素γ(interferon-γ,IFN-γ)等细胞因子的异常升高亦提示合并HLH可能[9]。
Ⅲ和Ⅳ期DLBCL患者的治疗以R-CHOP为一线化疗方案[2]。我们团队前期报道了一例以肝脾肿大、重度胆汁淤积为主要表现的DLBCL患者,在诊断明确时患者因重度黄疸(TBIL460.2 μmol/L,DBIL:433.7 μmol/L)住进消化专科ICU,及时启动R-CHOP方案化疗治疗,第一次化疗后肝功能指标迅速好转,化疗敏感性好,2周后肝功能指标基本恢复正常,肝脾形态基本恢复正常。随访至今已完成八次化疗,复查肝功指标未见异常,肝脾大小、密度恢复正常。故早期明确诊断DLBCL及早期化疗,患者预后较好。但该患者在明确诊断时出现严重噬血细胞综合征、肝功能衰竭、肠道功能衰竭等严重并发症,患者家属拒绝ICU器官支持治疗,自动出院后很快死亡。
综上所述,病理性脾梗死常见病因包括血栓栓塞疾病及血液良恶性疾病等,而地中海贫血、白血病、淋巴瘤是血液系统疾病中引起脾梗死最常见病因。当出现左上腹疼痛,腹部CT示片状或楔形低密度无强化区,其基底近脾的外缘,尖端指向脾门时,应考虑到脾梗死可能。淋巴瘤多以无痛性浅表淋巴结肿大为主要临床表现,以肝脾肿大、脾梗死、胆汁淤积为临床表现的较为罕见,故容易发生漏诊和误诊。在临床中,查体应仔细,在排除血栓栓塞及高凝状态等可能引起脾梗死病因外,需考虑是否有血液系统疾病,并及时完善骨髓、淋巴结活检。DLBCL早期诊断并及时化疗预后较好。而对于DLBCL患者病情快速进展需考虑是否为高级别B细胞淋巴瘤及合并淋巴瘤相关噬血细胞综合征等可能。
参考文献:
1. Chapman J, Helm TA, Kahwaji CI. Splenic Infarcts. 2023 Jul 17. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan–. PMID: 28613652
2. 中华人民共和国国家卫生健康委员会.淋巴瘤诊疗指南(2022年版).中国肿瘤临床与康复,2023,30(3):135-158.DOI:10.13455/j.cnki.cjcor.113494-20230316-0052.
3. Tokura, T, Murase, T, Toriyama, T, et al. Asian variant of CD5+ intravascular large B-cell lymphoma with splenic infarction. INTERNAL MED. 2003; 42 (1): 105-9. doi: 10.2169/internalmedicine.42.105.
4. Lawrence YR, Pokroy R, Berlowitz D, et al. Splenic infarction: an update on William Osler's observations. Isr Med Assoc J. 2010 Jun;12(6):362-5. PMID: 20928991.
5. 中华人民共和国国家卫生健康委员会.淋巴瘤诊疗指南(2022年版).中国肿瘤临床与康复,2023,30(3):135-158.DOI:10.13455/j.cnki.cjcor.113494-20230316-0052.
6. 中国抗癌协会淋巴瘤专业委员会,中华医学会血液学分会淋巴细胞疾病学组,中国噬血细胞综合征专家联盟.淋巴瘤相关噬血细胞综合征诊治中国专家共识(2022年版).中华医学杂志,2022,102(24):1794-1801.DOI:10.3760/cma.j.cn112137-20211109-02490.
7. 噬血细胞综合征中国专家联盟,中华医学会儿科学分会血液学组.噬血细胞综合征诊治中国专家共识.中华医学杂志,2018,98(2):91-95.DOI:10.3760/cma.j.issn.0376-2491.2018.02.004.
8. Henter, JI, Horne, A, Aricó, M, et al. HLH-2004: Diagnostic and therapeutic guidelines for hemophagocytic lymphohistiocytosis. PEDIATR BLOOD CANCER. 2007; 48 (2): 124-31. doi: 10.1002/pbc.21039.
9. Davis, EJ, Salem, JE, Young, A, et al. Hematologic Complications of Immune Checkpoint Inhibitors. ONCOLOGIST. 2019; 24 (5): 584-588.doi: 10.1634/theoncologist.2018-0574.

撰稿人
李春燕,西部战区总医院消化内科研究生,成都中医药大学硕士研究生在读。主要从事肝病临床研究。

撰稿人
常杏,消化内科主治医师,医学硕士,长期从事消化系统疾病诊疗工作。

撰稿人
黄爱萍,西部战区总医院病理科主治医师 ,成都高新医学会临床病理分会委员,四川省生物信息学学会精准医学分会委员。从事临床病理工作近10年,从事肝脏病理亚专业工作近6年,熟悉常见肝脏疾病的病理诊断及鉴别诊断。

审稿人
汤善宏,西部战区总医院消化内科主任
