本文来源:中华内科杂志, 2024,63(8) : 727-730.
本文作者:杨宏宇 吕继成 张宏
IgA肾病是全球范围内最常见的原发性肾小球疾病之一,在我国及东亚国家尤为常见。该病病理表现以IgA为主的免疫球蛋白在肾脏沉积,并导致系膜增生,临床以血尿为突出表现,伴有不同程度的尿蛋白或高血压,大多数患者表现为肾脏病缓慢进展,是导致青年人终末期肾病的最常见病因,给家庭和社会带来了沉重的疾病负担。近年来IgA肾病的治疗理念已有较大进步,基于发病机制的新药研发突飞猛进,而新的治疗措施亦将改变IgA肾病患者的最终结局。
一、IgA肾病治疗现状
既往大量研究普遍认为,仅约1/3的IgA肾病患者在发病10~20年后进展至终末期肾病。然而2023年来自英国全国罕见肾脏病登记系统的数据显示,基于现有治疗策略,50%的IgA肾病患者在10~15年内发生终末期肾病或死亡,而绝大多数患者均会在有生之年内发生肾衰竭。即使既往认为肾脏病进展低风险的人群,即尿蛋白控制在0.44~0.88 g/g(相当于尿蛋白0.5~1.0 g/d)的患者,仍会有高达30%的患者10年内进展为终末期肾病。近期一项分析我国IgA肾病患者长期预后的队列研究显示,尿蛋白控制良好的患者(0.5~1 g/d)中,22%的患者10年内发生肾衰竭;而尿蛋白持续超过1 g/d的患者,10年肾脏生存率仅为36%。上述研究均提示,基于现有的诊疗模式,IgA肾病患者的预后远比既往普遍认为的更为严峻。因此,IgA肾病的治疗急需新型药物,亦需要更新传统的治疗理念。
二、IgA肾病治疗观念的转变
传统IgA肾病的治疗策略主要是以支持治疗为基础,联合免疫抑制治疗。近年来IgA肾病发病机制的研究已取得巨大进展,尤其是我国及美国几项大型全基因组关联分析的研究结果,极大地提高了对该病发病机制的认识,为IgA肾病治疗新靶点的探索奠定了基础。在IgA肾病发病机制中,黏膜来源的IgA1,尤其是糖基化缺陷的IgA1,进入循环并形成以IgA为主的免疫复合物,这些大分子免疫复合物进而在肾小球系膜区沉积,引发补体旁路或凝集素途径激活及炎症反应,最终导致肾脏损伤,患者出现血尿、蛋白尿、肾功能下降等临床表现。基于这些发病机制,IgA肾病治疗主要有三种干预策略(图1):(1)在IgA肾病发病机制的源头上减少致病性IgA的产生,具体药物有:抑制肠道黏膜源性IgA产生的靶向释放糖皮质激素,如布地奈德靶向释放制剂(商品名耐赋康);抑制B淋巴细胞及浆细胞增生分化的B细胞活化因子(BAFF)和增殖诱导配体(APRIL)阻断剂,如泰他西普、阿塞西普;APRIL单克隆抗体,如sibeprenlimb、povetacicept、zigakibar,其均可抑制致病性IgA的产生并降低患者尿蛋白水平。(2)抑制肾脏局部炎症反应,包括系统性应用糖皮质激素、吗替麦考酚酯,未来亦可能包括补体阻断剂,尤其适用于肾脏病理中有活动性病变的IgA肾病患者。(3)支持治疗措施,主要通过降低肾小球滤过压和尿蛋白,延缓肾小球功能丢失,主要包括严格控制血压、限盐、血管紧张素转化酶抑制剂(ACEI)或血管紧张素受体阻断剂(ARB)类药物、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)、内皮素受体拮抗剂(MRA)等,尤其适用于肾脏慢性病变引起肾小球高滤过导致的蛋白尿的IgA肾病患者。由此可见,IgA肾病治疗策略正逐渐向多靶点的综合治疗策略转变,从传统糖皮质激素治疗时代走向基于发病机制的靶向治疗时代。
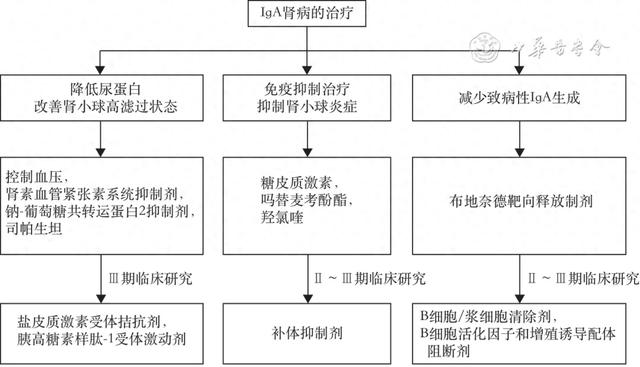
▲图1 IgA肾病的治疗策略
三、新药研发与进展
近半个世纪以来,IgA肾病治疗研究主要集中在支持治疗和糖皮质激素治疗,但现有的治疗策略下,大多数患者仍会在有生之年进展至终末期肾病。近年来IgA肾病新药研发有了较大的突破,尤其是在减少致病性IgA的产生及阻断补体激活方面取得了较大进展。随着新药到陆续上市,有望大幅度降低IgA肾病患者肾衰竭的风险,改善患者预后。
布地奈德靶向释放制剂治疗IgA肾病的Ⅲ期临床试验显示,与安慰剂比,布地奈德靶向释放制剂治疗12个月时,IgA肾病患者显著降低尿蛋白49.7%,随访两年时患者肾小球滤过率下降速率降低近50%(-6.1 ml·min-1·1.73m-2 比 -12.0 ml·min-1·1.73 m-2)。布地奈德靶向释放制剂是在回肠末端局部靶向释放布地奈德,可通过抑制肠道局部炎症反应,减少肠道来源的半乳糖缺陷的IgA1或IgA复合物,从IgA肾病发病机制源头上发挥治疗作用。目前该药已在全球(包括我国)批准用于高进展风险的IgA肾病的治疗。
APRIL单克隆抗体sibeprenlimab治疗IgA肾病的Ⅱ期临床试验显示,sibeprenlimab通过阻APRIL抑制B细胞介导的抗体生成和类别转换,抑制浆细胞分泌IgA产生。sibeprenlimab 每月8 mg/kg治疗IgA肾病患者 12个月,较安慰剂组显著降低尿蛋白42%。而BAFF和APRIL阻断剂泰他西普治疗IgA肾病的Ⅱ期临床试验显示,泰他西普每周240 mg 治疗IgA肾病患者6个月时,较安慰剂组显著降低尿蛋白52%,显示了良好的疗效。目前这些药物正在进行Ⅲ期临床试验。
在补体抑制剂中,补体替代途径B因子阻断剂(iptcopan)治疗IgA肾病的Ⅲ期临床试验的中期结果显示,与安慰剂比,iptacopan 200 mg 每日2次治疗IgA肾病患者9个月,显著降低尿蛋白38.3%,提示其具有良好的临床应用前景。但是凝集素途径的MASP-2单克隆抗体(OMS721)治疗IgA肾病的Ⅲ期临床试验(NCT03608033)的中期结果显示,治疗组和安慰剂组降尿蛋白的作用未达统计学意义,导致研究提前终止。其他补体通路抑制剂治疗IgA肾病的Ⅱ期或Ⅲ期研究亦在进行中。
四、我国在IgA肾病治疗策略发展中的贡献
相较于西方国家,IgA肾病在我国发病率高,患者人数较多,我国肾脏病学界在既往的十年为IgA肾病的治疗策略和新药研究作出了卓越的贡献,包括在新的糖皮质激素治疗方案、新的免疫抑制剂选择(羟氯喹、吗替麦考酚酯)、新型药物(泰他西普)研发等领域均达到国际先进水平,其研究成果影响了改善全球肾脏病预后组织(KDIGO)的国际肾小球肾炎指南的制订与更新。
2012年由我国北京大学第一医院肾内科牵头,包括澳大利亚、加拿大、印度、马来西亚共同参与的迄今为止最大的一项糖皮质激素治疗IgA肾病的国际多中心随机双盲对照研究(TESTING研究),共纳入503例具有高进展风险的IgA肾病患者,随访时间长达10年。该研究的第一阶段充分证实了足量糖皮质激素(甲泼尼龙0.8 mg·kg-1·d-1)方案可显著降低尿蛋白,并降低患者肾衰竭风险,澄清了IgA肾病糖皮质激素治疗无效论的争议,但同时患者出现较高比例包括严重感染在内的严重不良反应,缺乏绝对的临床获益。因此,第二阶段采取了减量糖皮质激素方案(甲泼尼龙0.4 mg·kg-1·d-1)联合复方磺胺类抗菌药物预防感染,结果显示,该治疗方案的疗效与足量糖皮质激素方案并无差别,将肾衰竭的风险降低了47%,而严重不良反应从16%降至5%,严重感染从8%降至4%,故提出一项安全有效的糖皮质激素治疗IgA肾病的新治疗策略,该方案亦获得国际认可,并被纳入KDIGO制订的肾小球肾炎指南中IgA肾病治疗的推荐。
在免疫抑制治疗领域,我国亦作出了突出的贡献。北京、香港、南京和广州分别牵头并最早完成的吗替麦考酚酯治疗IgA肾病的四项随机对照试验均证实,无论单独使用该药或联合糖皮质激素治疗,均可显著降低IgA肾病患者尿蛋白水平,长期随访显示,显著降低肾功能恶化的风险,尤其对伴有活动性病理改变的患者,应用吗替麦考酚酯可减少糖皮质激素用量及糖皮质激素不良反应。而我国亦最早探索了羟氯喹在IgA肾病治疗中的作用,由北京大学第一医院肾内科完成的目前唯一一项羟氯喹治疗IgA肾病的随机双盲对照试验显示,羟氯喹在支持治疗基础上可进一步显著降低IgA肾病患者的尿蛋白水平。基于此,KDIGO制订的肾小球肾炎指南亦推荐,包括羟氯喹和吗替麦考酚酯用于中国人IgA肾病治疗,并积极建议其他国家开展类似的临床研究。
我国在IgA肾病创新药物研发方面亦走在了国际前列。由我国研发的原创Ⅰ类新药泰他西普,率先在IgA肾病领域中开展了Ⅱ期临床试验,该药作为TACI受体与Fc的融合蛋白,可同时阻断BAFF对B细胞及APRIL对浆细胞的结合,抑制包括IgA在内的免疫球蛋白的产生,从而显示了非常广泛的治疗免疫疾病的应用前景,治疗IgA肾病的 Ⅱ期临床试验亦显示了良好的疗效和安全性,目前正在进行Ⅲ期临床试验,期待这一新药能大大改善IgA肾病患者的结局。
五、IgA肾病治疗的挑战与展望
近年来,我国IgA肾病无论在诊疗抑或新药研发方面均已取得较大进步,尤其是肾组织穿刺活检已普及至县一级以上医院,治疗总体水平亦有较大提升,但仍然面临全国范围内各地区发展不平衡的现状,并需要在以下方面进行提升:(1)肾脏病理诊断分型:牛津分型是由我国参与,并且是目前国际公认的病理分型系统,其评价系统的最大优点是可提示患者预后,并可以很好的区分急慢性病变,有助于免疫治疗方案的选择。但目前该分型系统普及率偏低,且需要提升分型的准确性。(2)治疗方案需要规范:目前在基层甚至某些大型三甲医院肾脏专科,存在肾素血管紧张素系统(RAAS)阻断剂使用率低,而糖皮质激素过度使用的情况,存在不结合患者临床表现、肾脏病理只要看到新月体病变即启动糖皮质激素治疗的误区,因此需要积极普及和推广目前国际指南推荐的IgA肾病治疗策略,提高以RAAS阻断剂为主的支持治疗的重视。糖皮质激素是一把双刃剑,在带来疗效的同时亦对患者带来较大的风险,因此需要结合患者临床情况和病理表现,合理把握糖皮质激素治疗的适应证;(3)不重视饮食控制,由于我国尤其北方人群普遍高盐摄入,且对青壮年患者而言,普遍以高盐的快餐作为饮食,极大影响了RAAS阻断剂疗效和尿蛋白的控制,需要积极的患者教育。
尽管我国近年来在IgA肾病治疗领域作出了突出贡献,但显然还是以传统治疗模式的更新为主,新药研发虽已有突破,但总体与西方发达国家比存在一定差距。因此需要我国肾脏病学界、基础医学及医药企业积极开展交叉融合研究,重视知识产权保护,改变以往单纯为研究成果发表为目的的研究模式,重视研究成果的转化。我科通过建立临床-基础-产业的联合实验室,研发了一种治疗IgA肾病的特异性新药——IgA重组融合蛋白酶,临床前实验显示可实现数小时内清除肾脏沉积的致病性IgA分子,明显优于现有其他研发中的药物,属于同类最优型的新药。希望未来我国积极寻求新的治疗靶点,研发更多的原研新药,真正将我国肾脏病新药研发达到国际领先水平。
本文编辑:胡朝晖
