在今年法国巴黎举行2023年全球肝炎峰会上(GHS-2023),研究人员以口头陈述方式介绍了Replicor公司研发的在研乙肝/丁肝新药REP 2139-Mg(皮下注射)的最新临床开发进展。

乙肝/丁肝GHS-2023,REP2139-Mg联合TDF,HDVRNA和HBsAg下降
研究课题:REP 2139-Mg联合富马酸替诺福韦二吡呋酯(TDF)治疗慢性丁肝和失代偿期肝硬化患者的安全性和有效性(已于今年4月28日在GHS-2023大会口头陈述)。
研究人员表示,慢性丁肝(CHD)是最严重的慢性病毒性肝炎之一,尽管已经对HBV治疗,但通常会观察到纤维化进展为肝硬化的情况。全球尚未批准对患有代偿期肝硬化的CHD患者采取抗病毒疗法。如果进展到失代偿期肝硬化,肝移植是唯一的选择。
在以往研究中,对因HDV引起的代偿期肝硬化使用REP2139-Mg通常具有良好的安全性。核酸聚合物(如REP2139)对HBV/HDV具有双重活性:此类新机制候选药物能够阻止HBV SVP从cccDNA或整合的HBVDNA组装,并阻止HDV SVP的包络。与HDAg的直接相互作用可能驱动观察到对HDV的上游抗病毒活性。
在已完成的2期临床开发证明了其对HBV和HDV的持久效果,具体可以通过两项试验深入了解,分别是在REP 401研究(针对HBV单一感染,治疗后5.3年):该研究中78%的患者免疫力得到控制,肝功能正常,肝脏僵硬度降低和或正常化,HBV功能性治愈率高达56%。
在REP 301研究中(针对HBV/HDV感染,治疗后7.4年):64%(7/11)HDVRNA水平检测不到,肝功能正常,肝脏僵硬度降低和或正常化。HBV功能性治愈有4名,部分治愈有3名。
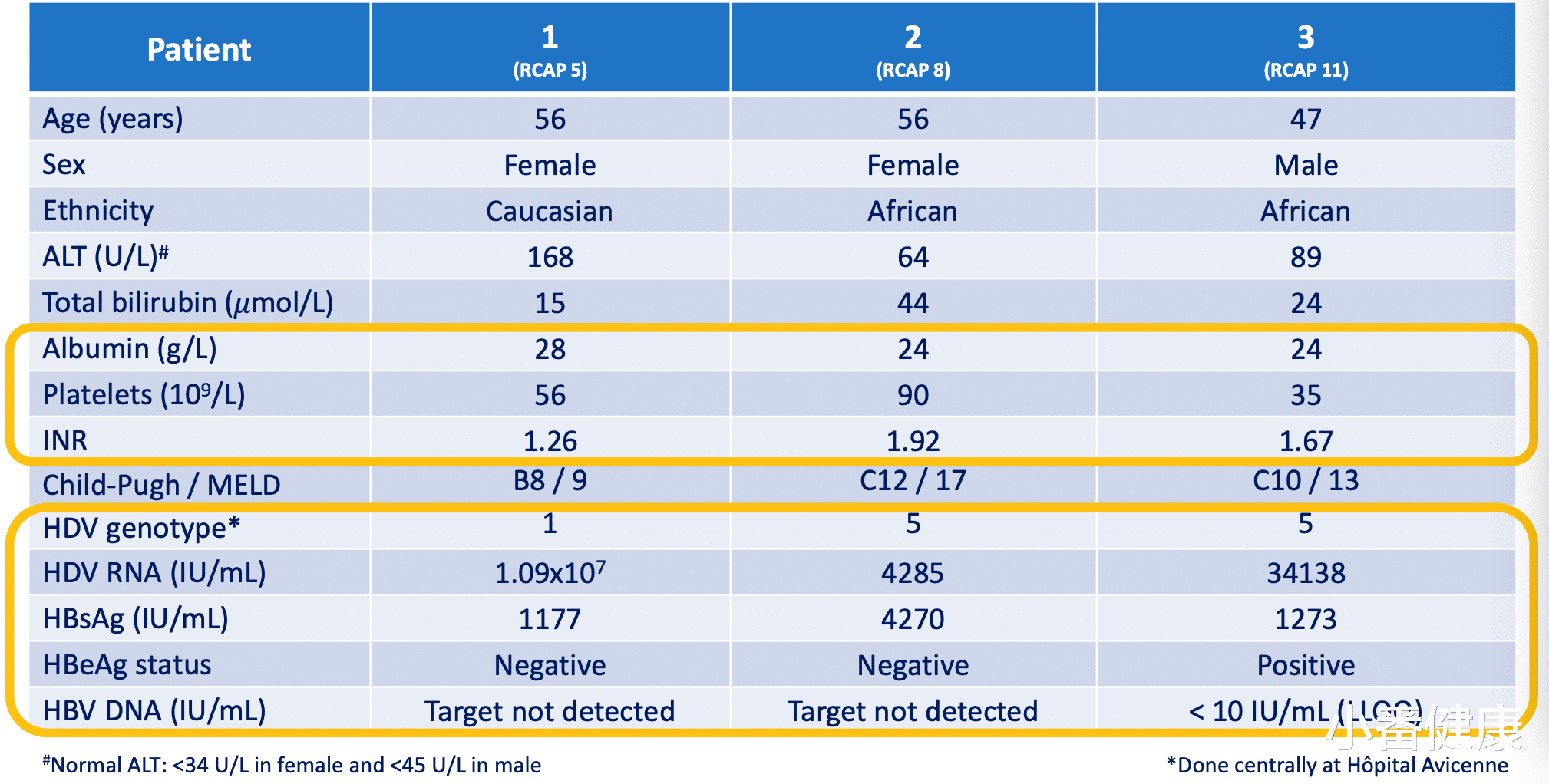
随后Replicor公司启动了一项同期用药计划,具体是在符合条件的受试者中同期使用REP 2139-Mg(RCAP,临床试验编号:NCT05683548)。这些受试者指以前对pegIFN、blevirtide和lonafarnib治疗失败的HBV/HDV患者。HBV/HDV失代偿期肝硬化,患有代偿期或失代偿期肝硬化的HBV患者。
当前全球各地区入组率:法国(18名,来自8个中心)——本研究提交的失代偿患者现有数据——以色列(1名,1个中心)、奥地利(3名,1个中心)、土耳其(4名,1个中心)、意大利(4名,1个中心)、德国(1名,1个中心)、澳大利亚(1名,1个中心)、加拿大(1名,1个中心)。
该同期计划目标是,评估REP2139-Mg对失代偿期肝硬化患者的有效性和安全性。所有受试者均接受计划时间为48周治疗:REP 2139-Mg 250 mg QW SC;TDF 245mg QD PO;在基线时收集临床和生物数据,前4周每周收集一次,然后每个月收集所有患者数据。
结果表明,没有血液学方面副作用,没有观察到ALT复发,没有与REP2139-Mg有关的一般副作用。该研究结论:在失代偿期肝硬化患者中,皮下注射(SC)REP 2139-Mg通常具有良好的耐受性和安全性。新的安全包络有可能将REP 2139-Mg的使用范围扩大到所有HBV和HBV/HDV患者;
观察到HDVRNA和HBsAg的下降,这一现象复制了在CHD代偿期肝硬化和以前临床试验中看到的一致下降结论。缺乏ALT/AST耀斑可能反映了肝硬化肝脏免疫状态的改变。将耀斑活动与REP2139的直接暴露脱钩。在失代偿期肝硬化患者中,功能性治愈HBV和HDV是可能的。

小番健康结语:近一年来,Replicor公司已启动同期用药计划(REP2139-Mg),以满足那些对现有疗法失败面临无药可用因HBV/HDV感染引起的失代偿期肝硬化患者。
药物研发技术方面,REP2139是一种核酸聚合物(NAP),核酸聚合物指寡核苷酸,它是通过独立于序列的寡核苷酸特性来发挥其生物效应。含有硫代磷酸酯修饰的NAP聚合物(其中非桥接氧被硫取代)有能力沿着暴露的两性α螺旋的暴露疏水表面退火并阻止构象变化。
作用机制方面,REP2139-Mg是通过直接和HDAg相互作用来抑制HDV复制,并通过抑制DNAJB12介导包络作用来阻断HDV释放。
