转自:药明康德
阿尔茨海默病(AD)是当下影响最为广泛的神经系统疾病之一,世界卫生组织预计全球患有痴呆症的人数已经超过5500万,其中AD是最常见的类型。现有研究已经知道β-淀粉样蛋白(Aβ)斑块和异常tau蛋白造成的神经缠结是AD的关键病理特征,而大多数AD疗法研究也是针对这两大特征开展的。
例如在2023年7月,美国FDA近20年来首次完全批准了一款阿尔茨海默病药物Leqembi(lecanemab),它就是通过靶向Aβ、清除毒性蛋白寡聚体来发挥作用。而在Aβ与tau蛋白靶点之外,其他的AD治疗思路仍然不多。
近期,麻省总医院和圣路易斯华盛顿大学合作带来了一种极其新颖的AD治疗策略:氙气疗法。研究者发现AD小鼠吸入氙气后,神经炎症水平明显下降,同时神经元受损风险降低。无论小鼠是具备Aβ还是tau蛋白神经缠结,氙气都能减轻AD的病理特征并改善AD症状。这将为AD治疗研究带来全新的思路和方向。

研究的共同通讯作者OlegButovsky博士表示:“当下许多药物难以穿透血脑屏障,但是氙气却能毫无阻拦进入大脑内部发挥作用。”这也是氙气疗法的一大优势。除此之外,氙气针对的目标更为特殊,它主要能恢复小胶质细胞的功能失调,从源头来阻止Aβ蛋白的累积。
小胶质细胞是大脑免疫系统的关键成员,它们能够积极响应感染、创伤并发挥吞噬作用,在大脑发育过程中还负责调节大脑功能。然而,AD患者的小胶质细胞通常扮演着“促炎”的角色,它们会引起神经炎症和氧化应激。科学家认为小胶质细胞炎症与Aβ会互相协同、形成恶性循环来加速神经损伤。过往一些研究提示,常用于麻醉的惰性气体——氙气可以帮助保护神经损伤,但鲜有研究探索氙气是否能影响AD的病理特征。
在实验中,研究者首先向小鼠的大脑皮层和海马体中注入了凋亡神经元,此举能够诱导小胶质细胞的聚集。他们发现,汇集而来的小胶质细胞会逐渐改变形态和特征,朝神经退行性小胶质细胞(MGnD)表型变化。MGnD会失去原本的“保护者”身份,其异常的免疫信号往往会促进局部炎症进展,损伤神经元。
但氙气的加入改变了这一局面。作者尝试让上述实验小鼠吸入了一定浓度的氙气,结果显示小胶质细胞开始转变、发挥出吞噬作用并减少了促炎表型。作者认为氙气进入大脑后,逆转了小胶质细胞的炎症表型,使其回退到了前神经退行性小胶质细胞(pre-MGnD)的状态。

并且,氙气不只是让小胶质细胞“改邪归正”,而是能帮助应对AD的发生与发展。作者分别选取了两类AD模型小鼠,一种具备淀粉样蛋白前体蛋白基因突变,会引起Aβ累积(APP/PS1小鼠);另一种具备APOE4突变,容易发展出tau蛋白神经缠结(P301S小鼠)。
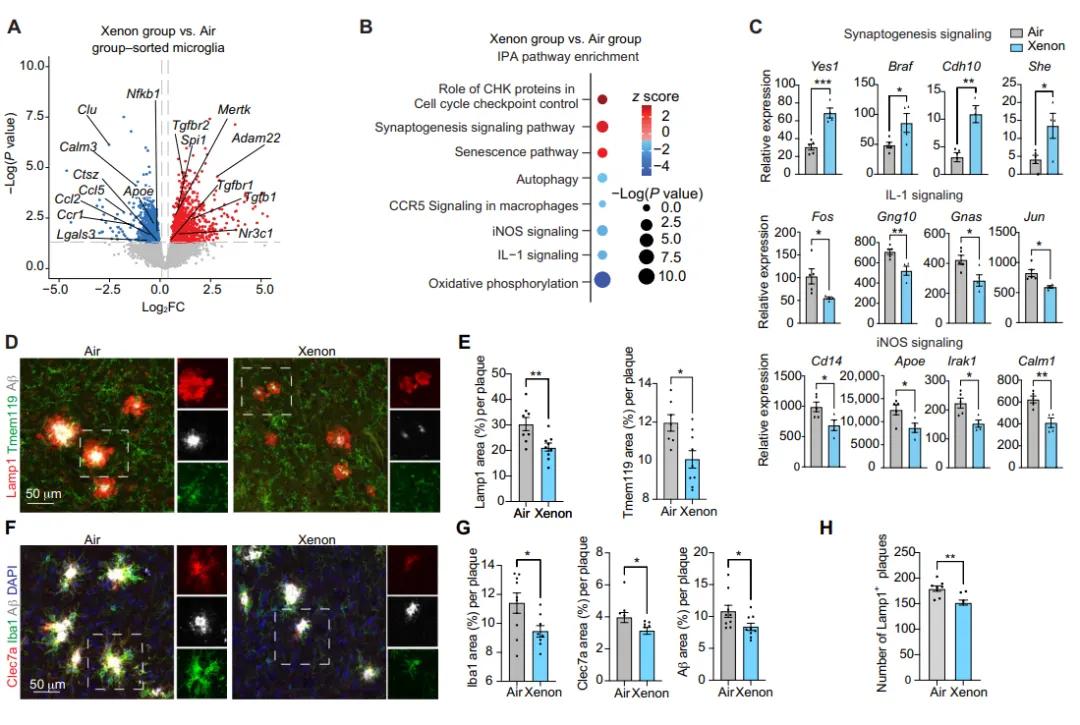
作者发现,两类小鼠在吸入氙气之后,大脑中的AD相关病理特征都会有所减轻:对APP/PS1小鼠来说,它们的小胶质细胞会逐渐减少炎症,并朝着pre-MGnD变化,微环境中的促炎因子水平降低,Aβ累积量减少;而P301S小鼠接受氙气治疗后,tau病理特征减少,维持了健康的齿状回厚度。另外,大脑中与神经、突触功能相关的基因表达上调,而与炎症相关基因表达下降。这些结果都展示出了氙气治疗策略的巨大潜力。
当然,氙气在人类应用中需要有着严格控制,而氙气是否能同样保护人类大脑仍需更多研究来探索。研究团队目前正在开展一项早期的临床试验,用于探索氙气疗法的安全性和剂量。如果被证实可行,AD患者将有望迎来一种全新且特殊的治疗策略。
参考资料:
[1]BrandaoW,etal.InhaledXenonmodulatesmicrogliaandamelioratesdiseaseinmousemodelsofamyloidosisandtauopathy.ScienceTranslationalMedicine,DOI:10.1126/scitranslmed.adk3690








