原创 CCMTV肿瘤频道
为了让我国临床肿瘤工作者能够更快、更方便地分享国际一流科研成果,中国临床肿瘤学会(CSCO)联合北京市希思科临床肿瘤学研究基金会共同主办的"2024年中国临床肿瘤学年度进展研讨会(BOC)暨 Best of ASCO 2024 China”于2024年7月5日至7日在广州召开。7月6日下午,Current Standard Practice after ASCO 2024作为压轴专场,江苏省人民医院的殷咏梅教授就乳腺癌领域的关键进展做了总结。CCMTV肿瘤频道将其内容整理成文,以飨读者。
HER2阳性乳腺癌
HER2+乳腺癌从“别无选择”到如今的如何在单克隆抗体、小分子TKI药物、ADC药物、新型ADC药物中选择,历经了二十多年。CSCO BC指南将HER2+乳腺癌分为曲妥治疗敏感和曲妥治疗失败两种类型进行分类而治,如图所示的路径图能够一目了然地指导我们的临床实践。然而这样的路径图还无法回答HER2+乳腺癌的所有问题。

第一个问题,基于现有药物,是否可以尝试新的治疗组合?
既往HER2CLIMB-02Ⅲ期随机对照研究已确证ADC+TKI的可行性。T-DM1+图卡替尼可显著改善经治HER2+MBC患者的PFS(9.5个月vs 7.4个月,HR0.76,P =0.0163)。联合治疗不良事件类型与既往报道一致,发生率略增加。
那么,抗HER2 ADC+帕妥珠单抗是否可行?今年ASCO上的DB07研究回答了这个问题。这是一个1b/2期、多中心、开放标签队列研究,三个队列分别是DS-8201单药、DS-8021联合免疫治疗、DS-8201联合帕妥珠单抗。尽管这只是一个1b/2期的临床研究,但是确实让我们看到DS-8201联合帕妥珠单抗的客观有效率高于DS-8201单药,与此同时,1+1>2的安全性值得我们关注。

DS-8201联合帕妥后,腹泻和贫血的发生率明显升高,联合治疗组≥3级AE的发生率提高了10%,间质性肺炎的发生率提高了5%。

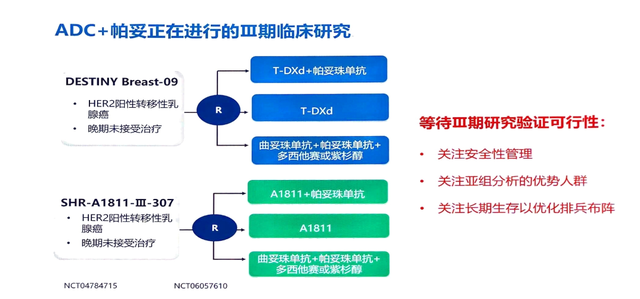
ADC联合帕妥的Ⅲ期临床研究DB09,这是一个德国的临床研究,江泽飞教授担任国内的leading PI,试图回答DS-8201单药,以及联合帕妥,和目前标准的一线治疗曲帕双靶进行对比。
SHR-A1811-m-307临床研究的研究内容和DB09类似,由江苏省人民医院担任组长单位。以上两项Ⅲ期临床研究未来可以回答ADC联合帕妥在有效性、安全性、优势人群,以及HER2+晚期乳腺癌的排兵布阵等方面的问题。
除了上述问题外,还有其他值得思考的问题。HER2+乳腺癌的一线治疗是紫杉类药物+HP,能否将紫杉换成其他化疗药,例如艾立布林?
艾立布林在中国和美国批准用于治疗既往接受过至少两种化疗方案(包括蒽环类和紫杉类)治疗的局部复发或转移性乳腺癌患者,在日本批准用于不能手术或复发的乳腺癌患者。

今年ASCO大会上我们看到了艾立布林的这方面探索,由日本专家主导的JBCGR-M06研究,一线艾立布林联合曲帕双靶和标准一线治疗紫杉类联合曲帕双靶头对头的比较,显示出非劣效性,同时3级不良事件的发生率较现在标准的紫杉联合双靶的副作用更小。

除此以外,针对HR+/HER2+晚期乳腺癌,是否可以去化疗?
早在2021年ASCO上,袁中玉教授的SYSUCC-002研究就验证了HR+/HER2+患者去化疗的可行性。在那个年代(2013-2019年),我们没有CDK4/6抑制剂,没有双靶,没有ADC药物,但这样一个化疗联合曲妥vs内分泌联合曲妥的Ⅲ期随机对照临床研究确实达到了非劣的结果。换句话说,针对肿瘤负荷小的HR+/HER2+乳腺癌患者,可以采用内分泌联合靶向的抗HER2治疗手段,指南也做了相应的推荐。

那么,针对HR+/HER2+乳腺癌患者,CDK4/6i+ET+抗HER2对比TPC效果如何?
今年ASCO上的PATRICIA研究就做了这样的探索,发现这样“去化疗”的手段达到了优效的结果,mPFS从对照组的7.5个月延长到了9.1个月。尽管CDK4/6抑制剂的加持带来的血液学毒性更高,但化疗带来的疼痛、呕吐的发生率要更低。


HER2阳性乳腺癌总结
一线治疗的最佳方案:
THPy和THP方依然是优先推荐方案。对于紫杉类治疗失败的患者可以考虑艾立布林;T-DXd和A1811一线治疗研究正在进行中;“ADC+”方案是否可以前移,有待更多数据优化排兵布阵方案,合理评估治疗获益、药物毒性和患者报告结局。强化内分泌去化疗方案的适用人群:
可以考虑PAM50等筛选从内分泌治疗的获益患者;PATINA研究探索一线6-8周期后维持治疗阶段+CDK4/6i的有效性,研究进行中。HR阳性乳腺癌
针对HR+EBC辅助治疗,2024 CSCO BC指南中,对于高复发风险的患者(淋巴结≥4个阳性,或者1-3个阳性同时伴有G3、T≥5cm、Ki67≥20%),基于MonarchE研究,指南将AI+阿贝西利作为一级推荐。
那么,淋巴结阴性的患者是否能从CDK4/6i的治疗中获益呢?MonarchE研究没法回答这个问题,因为它未入组N0患者。

而NATALEE研究研究入组了28%N0患者,在今年的ASCO大会上报告了N0亚组的iDFS,N0亚组瑞波西利治疗iDFS获益程度与总人群一致。但我们同时可以看到,由于N0患者相对低危,目前事件数比较少。瑞波西利3年的iDFS也仅仅带来了不到3%的获益,那么基于NATALEE研究,淋巴结阴性的患者是否要进行CDK4/6抑制剂的强化辅助呢?

就此问题,ASCO专家组认为:对于NATALEE试验中纳入的低风险患者特别是淋巴结阴性的乳腺癌患者,瑞波西利治疗的风险可能超过其获益。目前没有足够的证据明确哪些亚组一定不需要治疗,应该考虑每个患者的获益、风险成本和偏好。

2024 CSCO BC指南HR+MBC的部分,将晚期乳腺癌分5个分层,分别是:未经内分泌治疗、TAM治疗失败、NSAI治疗失败、SAI治疗失败、CDK4/6i失败。而国外的ABC5晚期乳腺癌诊疗指南有所不同,HR+MBC分层为:原发性内分泌耐药、继发性内分泌耐药、非内分泌耐药。

针对HR+MBC治疗策略,第一个问题,辅助内分泌治疗失败后,是否需要根据内分泌耐药情况进行分层治疗?
2023年SABCS,INAVO120研究在辅助内分泌治疗原发及继发耐药伴PIK3CA突变患者中探索Inavolisib+哌柏西利+氟维司群的疗效与安全性,三药联合PFS较对照组显著获益(15 vs. 7.3mo, HR:0.43)。
2024ASCO大会上披露了INAVO120 PFS2结果。Inavolisib 联合哌柏西利+氟维司群与疾病进展后的持续获益相关,显示后续抗肿瘤治疗需求的延迟(延迟8.9个月),包括化疗(NEvS.15.0个月),支持基于inavolisib的治疗方案的临床获益。
第二个问题,4种CDK4/6i在中国应用的真实世界数据?
目前晚期4种CDK4/6i获批,且疗效表现相似。以患者为中心,追求生活质量改善的前提下,CDK4/6i的报告结局表现值得关注。
由吴炅教授牵头的这项中国首个CDK4/6i的横断面研究,关注的是哌柏西利、阿贝西利、达尔西利的安全性和患者报告结局。患者问卷结果显示,达尔西利组的疲劳、脱发、潮热、失眠、关节痛、恶心、呕吐、腹泻、厌食发生率最低。

除此之外我们还需要回答的问题是,CDK4/6i进展后的治疗方案?
2022年ASCO,Ⅱ期MAINTAIN研究在CDK4/6抑制剂治疗失败患者(N=120)中探索了继续CDK4/6抑制剂维持治疗的可行性。瑞波西利组较安慰剂组延长PFS(5.29m vs 2.76m)。
2024年ASCO: Ⅲ期postMONARCH 研究入组CDK4/6i治疗失败晚期未接受其他治疗方案的患者,研究发现阿贝西利组较安慰剂降低27%的PFS事件风险。

除此以外,针对HR+/HER2低表达的患者,基于DB04研究中DS-8201在HER2低表达人群中的突出表现,我们改变了过去HER2+、HER2-的两分法,提出了HER2低表达这个概念。
今年ASCO上DB06研究数据公布,DB04、DB06研究均纳入的是HR+/HER2低表达的人群,DB06相较于DB04的区别在于:1、线数前移:DB04入组的是接受过一到二线化疗,而DB06中有一部分是一线CDK4/6i联合内分泌治疗6个月内进展的患者;2、DB06研究纳入超低表达患者:定义为≤10%的浸润癌细胞微弱的细胞膜染色(IHC>0<1+)。

DB06结果发现,在HER2低表达人群中,T-DXd组中位PFS为13.2个月,较TPC组延长5.1个月,疾病进展或死亡风险降低38%(HR=0.62,95% Cl:0.51-0.74)。在HER2超低表达人群的PFS改善与HER2低表达人群的获益一致。
DB-06表明T-DXd 是 HR+HER2低表达和超低表达≥1L内分泌治疗进展后的新选择。但T-DXd的适用人群是否能够拓展到“超低表达”面临病理检测标准的挑战。2022年FDA在批准DB04 HER2低表达时,同步批准了HER2蛋白检测抗体。说明病理检测一致性问题是适应症获批的考量因素。DB06中超低表达人群是否能够被监管部门认可有待观望。
HR阳性乳腺病总结
早期CDK4/6抑制剂适用人群:
高复发风险患者推荐CDK4/6抑制剂辅助治疗;淋巴结阴性患者结合疾病情况谨慎考虑。早期辅助内分泌治疗耐药(ABC5:原发、继发)人群:
内分泌治疗失败后,PIK3CA突变患者可考虑PI3K抑制剂+CDK4/6抑制剂+ET三药联合方案晚期CDK4/6抑制剂治疗失败后:
从研究数据角度:T-DXd方案取得优异的mPFS;但是否可以拓展到“超低表达”有待观望从药物可及性角度:换CDK4/6抑制剂跨线治疗是可选方案。从生物标志物角度:可考虑NGS检测针对PAM信号通路靶向治疗。三阴性乳腺癌
针对三阴性乳腺癌(TNBC),需要回答的问题很多,能够回答的问题却很少。
第一个问题,早期TNBC 免疫治疗的顺序是否重要?
Keynote 522研究,在新辅助和辅助阶段使用帕博利珠单抗,取得阳性结果。因此,2024 CSCO BC指南也将其纳入到了早期TNBC的新辅助免疫治疗、新辅助后辅助治疗中。

但是,Impassion 030研究,辅助阶段使用阿替利珠单抗,研究失败。在2024 ASCO 上,A-BRAVE研究针对高危人群辅助免疫治疗,虽然DFS数值上提高,但没有取得统计学差异。

为什么免疫治疗在TNBC新辅助以及晚期治疗阶段能够获得阳性结果,而在辅助阶段却是阴性的?
这可能是因为手术之后的肿瘤微环境的改变导致免疫治疗在辅助阶段的失败。
ADC新药与新组合
今年ASCO上有以下ADC新药研究值得我们关注:
首先是胡夕春教授担任leading PI的国产HER2-ADC ARX788 在HER2+mBC的Ⅲ期临床研究,ARX788相比拉帕替尼联合卡培他滨组显示出统计学显著性的PFS提升,OS尚不成熟,但显示出获益趋势。同时我们要关注到ARX788眼毒性和间质性肺炎的发生。


其次是国产的Trop-2 ADC药物,我们习惯称之为SKB264,OptiTROP-Breast01临床研究是针对晚期阶段≥2L抗肿瘤治疗的mTNBC,由徐兵河院士和我共同担任leading PI。与化疗相比,SKB264在PFS和OS方面均获得具有统计学意义和临床意义的改善。无论TROP2表达情况如何临床获益一致,TROP2高表达患者有更好的PFS趋势。
在安全性方面,SKB264和戈沙妥珠单抗(SG)在中国人群的数据是相似的。我们期待这款国产TROP2 ADC能够尽快在国内上市。

那么,未来这款TROP2 ADC是否可以联合免疫治疗呢?“协同”是否“增效”还有待临床研究来验证。
现有的戈沙妥珠单抗联合帕博利珠单抗治疗≥1L的HR+HER2-mBC,以及Dato-TXd联合度伐利尤单抗新辅助治疗HER2-EBC,仅仅在数值上有改善,但未达到统计学的差异。

我们期待正在进行的TROPION-Breast 04(Ⅲ期,Dato-Dxd+度伐利尤单抗,TNBC早期)、TroFUSE-010(Ⅲ期,SKB264+帕博利珠单抗,HR+HER2-晚期)、TroFUSE-012(Ⅲ期,SKB264+帕博利珠单抗,TNBC早期)能够回答这个问题。
以上就是2024ASCO的最新研究给我们临床实践带来的改变。
