于3月份获得美国FDA批准的口服甲状腺激素受体(THR)-β选择性激动剂Rezdiffra(通用名为resmetirom)现已在美国上市。
该药物可与饮食和运动结合使用,用于治疗患有中度至晚期肝纤维化(与F2至F3期纤维化一致)的成人非肝硬化非酒精性脂肪性肝炎(NASH)。
根据3期MAESTRO-NASH研究(NCT03900429)的数据,该治疗获得了加速批准。研究结果显示,与安慰剂相比,Rezdiffra组中纤维化改善和NASH消退的患者比例更高。
Rezdiffra最常见的不良反应包括腹泻、恶心、瘙痒、呕吐、便秘、腹痛和头晕。处方信息还包括与肝毒性和胆囊相关不良反应相关的警告和注意事项。中度至重度肝功能损害患者应避免使用Rezdiffra。
不建议将Rezdiffra与强CYP2C8抑制剂以及有机阴离子转运多肽(OATP)1B1和OATP1B3抑制剂同时使用。与中度CYP2C8抑制剂同时使用时,应减少Rezdiffra的剂量。如果Rezdiffra与CYP2C8底物共同给药,则应更频繁地监测患者是否有底物相关的不良反应,其中最小的浓度变化可能会导致严重的不良反应。
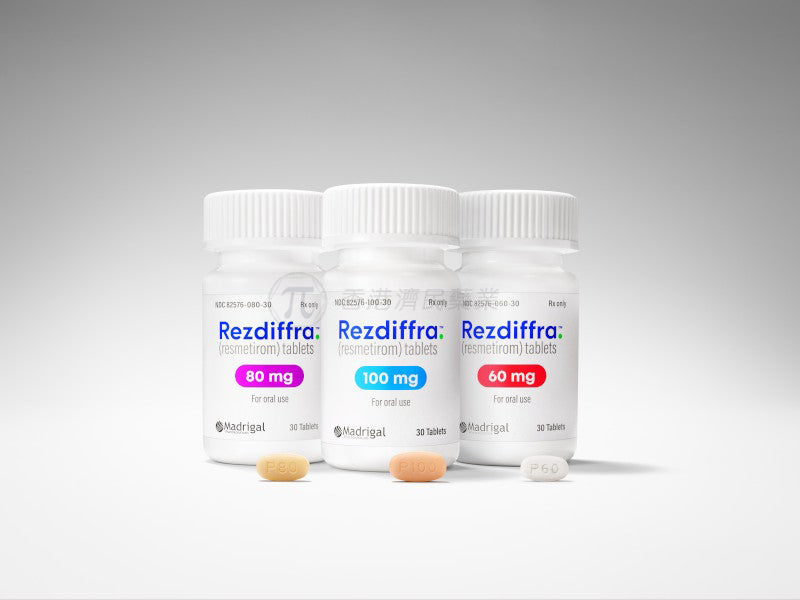
Rezdiffra的片剂剂量强度有60mg、80mg和100mg。根据药物标签,其推荐剂量根据实际体重而定。对于体重小于100kg的患者,推荐剂量为80mg,每日一次口服。对于体重至少100kg的患者,推荐剂量为每日一次口服100mg。
参考来源:‘Madrigal Pharmaceuticals Announces U.S. Availability of Rezdiffra™ (resmetirom) for the Treatment of Patients with Noncirrhotic NASH with Moderate to Advanced Liver Fibrosis’,新闻稿。Madrigal Pharmaceuticals;2024年4月9日发布。
注:本文旨在介绍医药健康研究,不作任何用药依据,具体用药指引,请咨询主治医师。

上哪找100kg的患者?