免疫治疗的出现彻底改变了我们对抗癌症的方式,它通过激活人体的免疫系统,使得T细胞能够精准且持久地攻击肿瘤细胞,为那些原本无望的晚期患者带来了新的希望。
这场医学革命的先锋就是免疫检查点抑制剂(ICI),它们通过解除免疫系统的“刹车”,让T细胞全力以赴,对肿瘤细胞发起猛烈攻击,在多种癌症的治疗中取得了前所未有的成功。例如,大家耳熟能详的K药(帕博利珠单抗)、O药(纳武利尤单抗)、T药(阿替利珠单抗)等等。
然而,药物总有两面性。过度激活的免疫系统不仅会瞄准肿瘤细胞,也可能误伤正常的组织和器官,带来严重的副作用。虽然某些免疫不良反应,如皮肤毒性的出现,有时反而是治疗有效的信号,但我们今天要讨论心脏毒性,它就像一颗潜伏在体内的致命炸弹。
心脏毒性(CVAEs)表现多样,包括心肌炎、心包炎、急性冠脉综合征、心力衰竭、心律失常、传导异常,甚至是心脏骤停。尽管这些情况相对罕见,但其危险性极高,尤其是心肌炎,死亡率竟可高达4成!
近期,《JAMA Oncology》刊登了一项纳入8万多人,涵盖了589项试验的荟萃分析,揭示了ICIs相关心脏毒性的发生率,并深入探讨了如何更有效地识别和管理这些潜在的致命事件。
免疫治疗的潜在隐忧, 识别心脏毒性高危因子ICI引起心脏毒性的总体发生率均不高,但通过分析之后,研究者们发现了一些重要的差别:
接受PD-1抑制剂或PD-L1抑制剂后所有级别心脏毒性发生率为1.07%、0.63%;高级别(3-4级)毒性发生率为0.69%、0.40%。
在PD-1/PD-L1抑制剂以及CTLA-4抑制剂中,除西米普利单抗(Cemiplimab)外,不同药物间心脏毒性发病率无显著差异。
而西米普利单抗与更高的心脏毒性风险相关(p<0.001),其心脏毒性发生率为3.77%,高级别心脏毒性发生率为2.91%。
接受双免治疗的患者,心肌炎的发生率显著增加。不过,双免、ICIs联合化疗(除蒽环类)或酪氨酸激酶抑制剂(TKIs)并未导致更高的心脏毒性发生率。而在与蒽环药物联合使用时要格外注意心脏毒性的监控。
具体的药物如图所示:

心脏毒性发病率
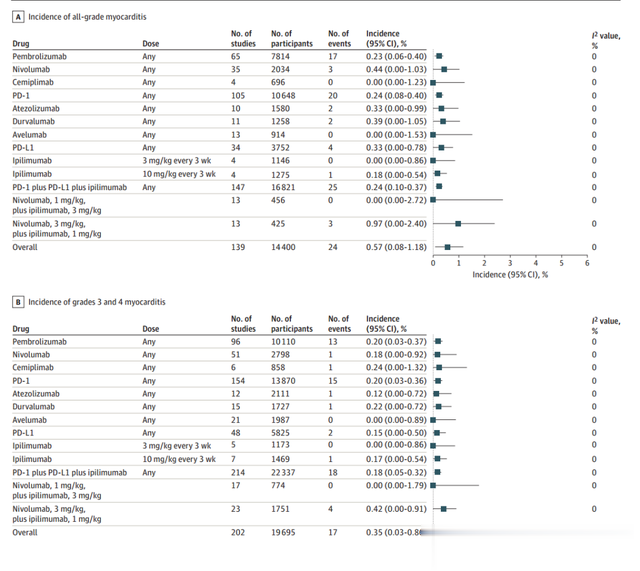
心肌炎发病率
死亡率接近4成, 如何制止这一致命杀手该研究的第二部分探讨了心肌炎相关死亡率的严重性。回顾性分析和个案报告显示,在220例ICIs诱发的心肌炎病例中,有83例患者(37.7%)死亡。
因此,需要对接受治疗的患者进行监控,尤其是在早期,该研究指出接受ICI治疗后至出现心脏毒性的中位时间为23.5天。对于ICI抑制剂相关的心脏毒性事件,诊断通常需要进行全面的检查,包括心电图、超声心动图、胸部X光片、心肌酶检测以及心脏磁共振成像等。
而一旦发现,停止ICI治疗、开始皮质类固醇治疗、通过遥测监测进行支持治疗以及升级到重症监护病房进行正性肌力和机械循环支持是治疗心肌炎的关键要素。
由于ICIs相关心肌炎可能导致危及生命的恶性心律失常或合并心力衰竭的暴发性心肌炎,我国《2023 CSCO肿瘤心脏病学临床实践指南》建议所有可疑及确诊的所有级别心肌炎均暂停ICIs治疗,并针对毒性严重程度采取分级治疗。严重心肌炎患者如果糖皮质激素治疗24h无缓解,应尽早考虑使用免疫抑制剂+和血浆置换±生命支持。
本研究作者指出阿巴西普(Abatacept)治疗ICI心肌炎的成功率超过90%,因此建议作为治疗首选药物,并且阿巴西普与JAK激酶抑制剂联合使用可能更有效。
总之,对于正在接受免疫治疗的患者来说,了解这些潜在风险是至关重要的。与医生密切合作,定期进行检查和监控,可以在早期发现问题并采取适当的应对措施,最大限度地降低心脏毒性风险。
参考文献:
[1]. Yamani N, Ahmed A, Ruiz G, Zubair A, Arif F, Mookadam F. Immune checkpoint inhibitor-induced cardiotoxicity in patients with lung cancer: a systematic review and meta-analysis. Cardiooncology. 2024 Jun 17;10(1):37.
[2]. 2023 CSCO肿瘤心脏病学临床实践指南
