Bepirovirsen(GSK3228836)是一种在研乙肝病毒反义寡核苷酸(ASO),GSK公司等科研人员最近介绍了一项最新研究进展。

乙肝在研新药GSK836,评估支持临床剂量选择,小鼠及首次1期公布
该研究指反义寡核苷酸Bepirovirsen在乙肝病毒转基因小鼠和人类健康受试者中的临床前和1期临床试验评估:支持临床剂量选择和单剂量、多剂量的安全性、耐受性和药代动力学评估。
据估计,2016年有2.92亿人患有慢性乙型肝炎病毒 (HBV) 感染。以肝脏炎症为特征的慢性HBV会增加肝硬化和肝细胞癌发展并导致死亡的风险。核苷(酸)类似物(NAs)是目前全球的慢性HBV一线疗法,因为它们能够有效抑制HBVDNA水平并降低疾病并发症的可能性。
然而,这种一线疗法在对乙肝表面抗原(HBsAg;慢性感染的标志)的清除很少发生,即使长期治疗也可能不会导致HBsAg消失/防止复发。据推测,HBsAg通过抑制宿主免疫反应在病毒持久性中起主要作用;HBsAg抑制可能允许免疫反应的重建。
在临床前研究中,无论是单药治疗还是与核苷类组合使用,靶向HBV基因组区域的反义寡核苷酸均可有效降低血清 HBsAg 和 HBVDNA。(GSK3228836),以往名为 ISIS 505358 或 IONIS-HBVRx,是一种 2'-O - 甲氧基乙基 (2'-MOE) 修饰的反义寡核苷酸正用于治疗慢性HBV感染的临床开发中。GSK836结合位点存在于HBV 信使RNA(mRNA)中,包括前基因组RNA(pgRNA),并在整个基因组中高度保守HBV基因型;因此,GSK836有望通过RNase H1 机制来降低 HBV mRNA 和 pgRNA 的水平。

GSK836是从一组 HBV 靶向反义寡核苷酸候选物中选择的,基于其在体外和体内降低HBsAg水平的效力HBV表达系统及其在小鼠和猴子中的安全性和耐受性。在首次人体1期研究之前进行的GSK836非临床研究中,未观察到意外毒性。在一般毒理学研究中,研究了GSK836的血浆PK和组织分布情况,结果与其他 2'-MOE 反义寡核苷酸观察到结果一致。
在本研究中,报告了体外和体内研究结果,这些结果为GSK836在人体研究中的剂量选择提供了信息。研究人员还提供了GSK836首个人体1期临床试验(研究 213725;ISIS 50538-CS1)数据,该研究评估了在健康受试者中使用GSK836单剂和多剂的 PK、安全性和耐受性。
GSK836旨在靶向HBV基因组的一个高度保守区域。在临床前研究中,GSK836 减少了细胞内HBVRNA和DNA复制中间体,这反映在HBV表达中分泌的 HBsAg 和 HBeAg的减少以及HBV转基因小鼠模型中的病毒粒子DNA。这表明病毒复制减少,与关键病毒蛋白以及作为病毒复制模板的HBV pgRNA(3.5-kb 转录物)的减少一致。
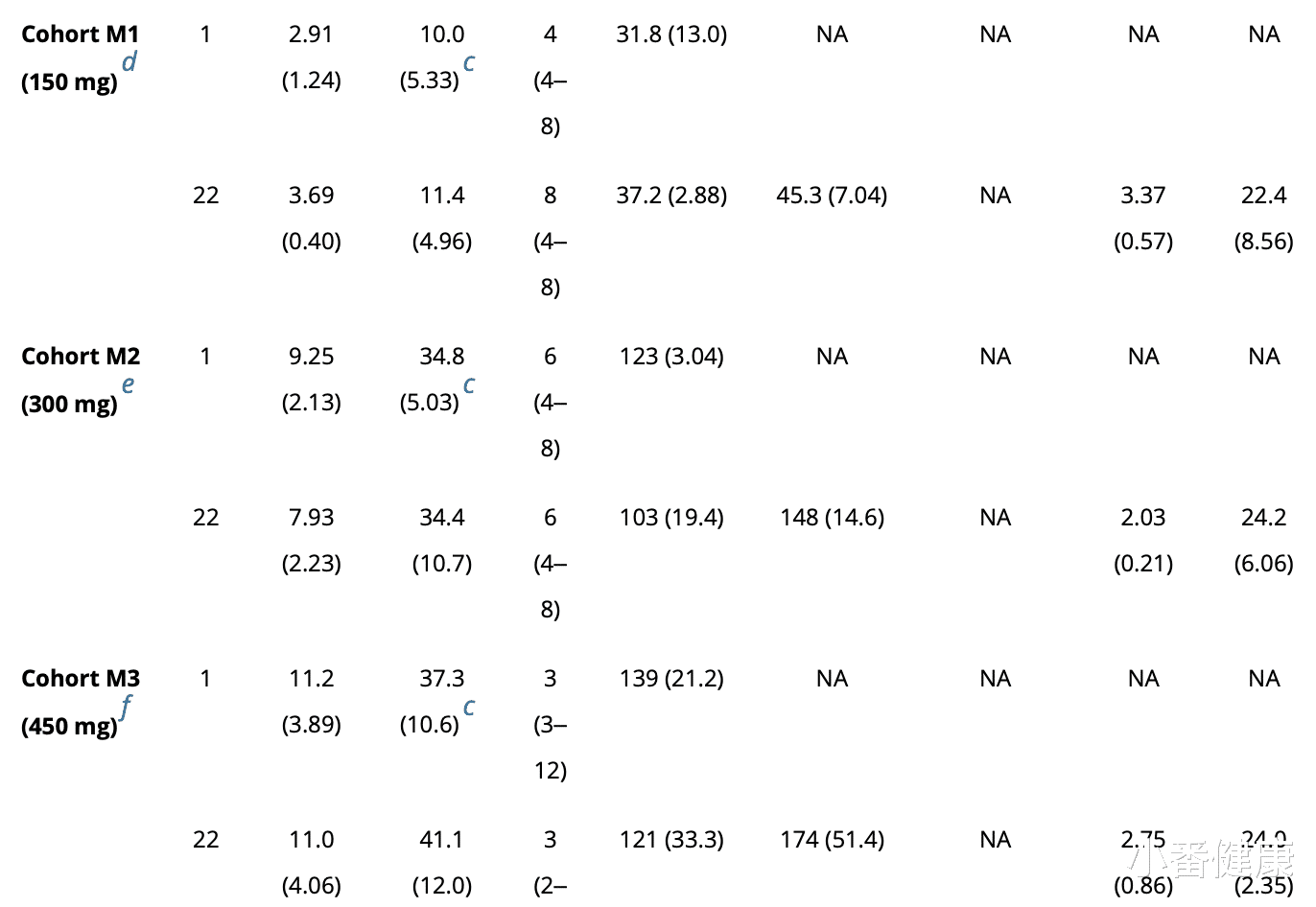
这些数据表明,在预测的临床剂量下,有效的抗病毒药物和HBsAg降低是可行的。GSK836的临床疗效评估是未来研究的重要途径,目前正在治疗慢性HBV感染的临床试验评估中。在当前的1期首次人体研究中,健康受试者的血浆PK曲线表征表明,GSK836倍迅速吸收到体循环中,在单剂量和多剂量 SC 给药后 3-8小时观察到Cmax。

血浆暴露随着剂量的增加而增加,并在较高剂量(150-450 mg)下似乎与剂量成正比,重复给药后几乎没有积累。多剂量组中GSK836的血浆谷浓度也随着剂量的增加而增加,这反映了组织暴露。由于负荷剂量方案,到第 22 天迅速达到稳态浓度。对于全长GSK836而言肾脏清除是次要的消除途径,尿液中排出的总剂量<2%。与单次剂量相比,在多次给药后观察到更高的尿排泄,表明与先前剂量相关的寡核苷酸的累积尿排泄。预计消除的主要途径是核酸酶介导的组织代谢和GSK836链缩短代谢物的尿排泄。
2'-MOE 反义寡核苷酸药物类别的成员具有相似的物理化学性质,导致相似的 PK 行为。GSK836的血浆浓度快速下降和全长药物的肾消除水平较第一个24 小时与该化学类别的化合物的预期一致,并且与分布到组织而不是消除/排泄一致。整个药物类别的这一观察结果以及GSK836的长半衰期支持每周给药方案。
在这项 1 期研究中对安全性和耐受性的评估没有发现任何会阻止该化合物进一步开发的安全性信号,在单剂量和多剂量队列中,99% 因治疗出现的 AE 的严重程度属于轻微级。大多数治疗出现的 AE 与注射部位的局部 SC 反应有关 (65%)。在单剂量和多剂量队列中观察到 CRP 无症状升高。数据表明,单剂量可以诱导 CRP 升高,但后续剂量的GSK836不会加剧这些情况。
在一些但不是全部 2'-MOE 反义寡核苷酸给药后观察到瞬时 CRP 增加。因此,尚不清楚早期 CRP 增加是否是药物类效应,但应在未来的 2'-MOE 研究中监测反义寡核苷酸。在这项研究中观察到 ALT 的轻微无症状升高。有 1 名受试者的 ALT 升高至≤2.6 × ULN,而总胆红素没有临床相关变化,并且不需要中断给药。美国食品和药物管理局(FDA)关于药物性肝损伤的指南指出,与对照组相比,ALT 升高 > 3 × ULN 可能是肝损伤可能性的有用指标。研究中没有受试者达到该 ALT 阈值。
然而,鉴于样本量小,有必要继续评估肝脏化学以排除药物性肝损伤的可能性。虽然反义寡核苷酸通常不会观察到临床相关的 ALT 升高,但 mipomersen 和 ISIS 449884 观察到 ALT 升高,可能与它们的药理作用有关,即抑制 apoB100 和胰高血糖素受体。
总体而言,这项首次人体研究的结果表明,当健康受试者以单剂和多剂形式给予GSK836时,表现出可接受的安全性,其血浆 PK 曲线与其他 2'-MOE 反义寡核苷酸相似。临床前实验支持在 1 期研究中评估的剂量下具有有效的抗病毒活性。这些结果支持在慢性乙肝受试者中进一步评估每周剂量高达 450 毫克的GSK836。

核心结论及数据:在HepG2.2.15细胞中,观察到使用GSK836后,HBVRNA、HBVDNA和病毒蛋白(乙肝表面抗原)的剂量依赖性减少。在以 50 mg/kg/wk 治疗的HBV转基因小鼠中,肝脏HBVRNA和DNA分别减少了 90% 和 99%。
随后,在一项首次人体第1期临床研究中对96名健康受试者给予GSK836。结果表明,所有剂量水平的GSK836都被迅速吸收(给药后3-8小时达到最大血浆浓度),迅速分布到外周组织,并缓慢消除(中位血浆终末半衰期:22.5-24.6天跨组)。在第一次和第六次给药后,血浆暴露(150-450mg 的剂量比例)和浓度-时间曲线相似,这表明几乎没有血浆蓄积(到第22天达到稳定状态)。

全长GSK836的肾消除占总剂量 <2%。在单剂量和多剂量队列中,报告了 197 起治疗中出现的不良事件,其中 99% 和 65% 的严重性和局部注射部位反应分别为轻度。总之,GSK836在人体中显示出可接受的安全性,观察到的药代动力学与化学类别一致,值得进一步评估GSK836在慢性HBV感染中的作用。
以上是在研乙肝反义寡核苷酸GSK836最新进展,进展来自《药物开发临床药理学》Clinical Pharmacology in Drug Development。

最有希望的临床治愈药,大概什么时候能上市?